مشخصه انرژی درونی بدن چیست؟ تغییر در انرژی درونی
در نظر گرفتن یک پدیده فیزیکی خاص یا دسته ای از پدیده ها با استفاده از مدل هایی با درجات مختلف تقریب راحت است. به عنوان مثال، هنگام توصیف رفتار یک گاز، از یک مدل فیزیکی استفاده می شود - یک گاز ایده آل.
هر مدلی محدودیتهایی برای کاربرد دارد که فراتر از آن نیاز به توضیح یا استفاده از گزینههای پیچیدهتر دارد. در اینجا ما یک مورد ساده از توصیف انرژی داخلی یک سیستم فیزیکی را بر اساس ضروری ترین خواص گازها در محدوده معین در نظر خواهیم گرفت.
گاز ایده آل
برای سهولت در توصیف برخی از فرآیندهای اساسی، این مدل فیزیکی یک گاز واقعی را به صورت زیر ساده می کند:
- اندازه مولکول های گاز را نادیده می گیرد. این بدان معنی است که پدیده هایی وجود دارند که این پارامتر برای توصیف کافی برای آنها ضروری نیست.
- از فعل و انفعالات بین مولکولی غفلت می کند، یعنی می پذیرد که در فرآیندهای مورد علاقه در دوره های زمانی بسیار ناچیز خود را نشان می دهند و بر وضعیت سیستم تأثیر نمی گذارند. در این حالت، فعل و انفعالات دارای ماهیت یک ضربه کاملاً الاستیک هستند که در آن هیچ اتلاف انرژی به دلیل تغییر شکل وجود ندارد.
- از تعامل مولکول ها با دیواره های مخزن غفلت می کند.
- فرض بر این است که سیستم مخزن گاز با تعادل ترمودینامیکی مشخص می شود.
این مدل برای توصیف گازهای واقعی در صورتی که فشار و دما نسبتاً پایین باشد مناسب است.
وضعیت انرژی یک سیستم فیزیکی
هر سیستم فیزیکی ماکروسکوپی (بدن، گاز یا مایع در یک ظرف)، علاوه بر جنبشی و پتانسیل خود، نوع دیگری از انرژی - داخلی دارد. این مقدار با جمع کردن انرژی تمام زیرسیستم های تشکیل دهنده سیستم فیزیکی - مولکول ها به دست می آید.
هر مولکول در گاز نیز پتانسیل و انرژی جنبشی خاص خود را دارد. مورد دوم به دلیل حرکت حرارتی بی نظم مداوم مولکول ها است. فعل و انفعالات مختلف بین آنها (جاذبه الکتریکی، دافعه) توسط انرژی پتانسیل تعیین می شود.
باید به خاطر داشت که اگر وضعیت انرژی هر یک از بخشهای یک سیستم فیزیکی هیچ تأثیری بر وضعیت ماکروسکوپی سیستم نداشته باشد، در نظر گرفته نمیشود. به عنوان مثال، در شرایط عادی، انرژی هسته ای خود را در تغییر وضعیت یک جسم فیزیکی نشان نمی دهد، بنابراین نیازی به در نظر گرفتن آن نیست. اما در دماها و فشارهای بالا این کار باید انجام شود.
بنابراین، انرژی درونی یک جسم ماهیت حرکت و تعامل ذرات آن را منعکس می کند. این بدان معنی است که این اصطلاح مترادف با مفهوم اغلب مورد استفاده "انرژی حرارتی" است.
گازهای تک اتمی، یعنی آنهایی که اتمهای آنها در مولکولها ترکیب نمی شوند، در طبیعت وجود دارند - اینها گازهای بی اثر هستند. گازهایی مانند اکسیژن، نیتروژن یا هیدروژن تنها در شرایطی می توانند در چنین حالتی وجود داشته باشند که انرژی از بیرون صرف شود تا دائماً این حالت تجدید شود، زیرا اتم های آنها از نظر شیمیایی فعال هستند و تمایل دارند به یک مولکول ترکیب شوند.

اجازه دهید وضعیت انرژی یک گاز ایده آل تک اتمی را در ظرفی با حجمی در نظر بگیریم. این ساده ترین حالت است. به یاد داریم که برهمکنش الکترومغناطیسی اتم ها با یکدیگر و با دیواره های ظرف و در نتیجه انرژی پتانسیل آنها ناچیز است. بنابراین انرژی داخلی یک گاز فقط شامل مجموع انرژی جنبشی اتم های آن می شود.
می توان آن را با ضرب میانگین انرژی جنبشی اتم های گاز در تعداد آنها محاسبه کرد. انرژی متوسط برابر است با E = 3/2 x R / N A x T، که در آن R ثابت گاز جهانی است، N A عدد آووگادرو، T دمای مطلق گاز است. تعداد اتم ها را با ضرب مقدار ماده در ثابت آووگادرو محاسبه می کنیم. انرژی داخلی یک گاز تک اتمی برابر با U = N A x m / M x 3/2 x R / N A x T = 3/2 x m / M x RT خواهد بود. در اینجا m جرم و M جرم مولی گاز است.
فرض کنید ترکیب شیمیایی گاز و جرم آن همیشه ثابت بماند. در این حالت همانطور که از فرمولی که به دست آوردیم مشخص است، انرژی داخلی فقط به دمای گاز بستگی دارد. برای یک گاز واقعی، علاوه بر دما، تغییر حجم نیز لازم است، زیرا این بر انرژی پتانسیل اتم ها تأثیر می گذارد.
گازهای مولکولی
در فرمول فوق، عدد 3 تعداد درجات آزادی حرکت یک ذره تک اتمی را مشخص می کند - با تعداد مختصات در فضا تعیین می شود: x، y، z. برای وضعیت یک گاز تک اتمی، به طور کلی بی تفاوت است که اتم های آن بچرخند.
مولکول ها از نظر کروی نامتقارن هستند، بنابراین، هنگام تعیین وضعیت انرژی گازهای مولکولی، لازم است انرژی جنبشی چرخش آنها در نظر گرفته شود. مولکول های دو اتمی، علاوه بر درجات آزادی ذکر شده مرتبط با حرکت انتقالی، دارای دو درجه دیگر با چرخش حول دو محور عمود بر هم هستند. مولکول های چند اتمی دارای سه محور چرخش مستقل هستند. در نتیجه، ذرات گازهای دو اتمی با تعداد درجه آزادی f = 5 مشخص می شوند، در حالی که برای مولکول های چند اتمی f = 6.

با توجه به تصادفی بودن ذاتی حرکت حرارتی، همه جهات حرکت چرخشی و انتقالی کاملاً به یک اندازه محتمل هستند. میانگین انرژی جنبشی ارائه شده توسط هر نوع حرکت یکسان است. بنابراین، می توانیم مقدار f را در فرمول جایگزین کنیم، که به ما امکان می دهد انرژی داخلی یک گاز ایده آل از هر ترکیب مولکولی را محاسبه کنیم: U = f / 2 x m / M x RT.
البته از فرمول می بینیم که این مقدار به مقدار ماده یعنی اینکه چقدر و چه نوع گازی گرفته ایم و همچنین به ساختار مولکول های این گاز بستگی دارد. با این حال، از آنجایی که ما توافق کردیم که جرم و ترکیب شیمیایی را تغییر ندهیم، فقط باید دما را در نظر بگیریم.
حالا بیایید ببینیم که چگونه مقدار U با سایر مشخصات گاز - حجم و فشار - مرتبط است.
انرژی داخلی و حالت ترمودینامیکی
دما همانطور که مشخص است یکی از حالات سیستم (در این مورد گاز) است. در یک گاز ایده آل، با رابطه PV = m / M x RT (به اصطلاح معادله Clapeyron-Mendeleev) با فشار و حجم مرتبط است. دما تعیین کننده انرژی حرارتی است. بنابراین مورد دوم را می توان از طریق مجموعه ای از پارامترهای حالت دیگر بیان کرد. او نسبت به حالت قبلی و همچنین به روش تغییر آن بی تفاوت است.
بیایید ببینیم که انرژی داخلی چگونه تغییر می کند وقتی یک سیستم از یک حالت ترمودینامیکی به حالت ترمودینامیکی دیگر حرکت می کند. تغییر آن در طول چنین انتقالی با تفاوت بین مقادیر اولیه و نهایی تعیین می شود. اگر سیستم پس از چند حالت میانی به حالت اولیه خود برگردد، این اختلاف برابر با صفر خواهد بود.

فرض کنید گاز را در مخزن گرم کردیم (یعنی انرژی اضافی برای آن تامین کردیم). حالت ترمودینامیکی گاز تغییر کرد: دما و فشار آن افزایش یافت. این فرآیند بدون تغییر صدا انجام می شود. انرژی داخلی گاز ما افزایش یافته است. پس از این، گاز ما انرژی عرضه شده را رها کرد و به حالت اولیه خنک شد. عاملی مانند سرعت این فرآیندها هیچ اهمیتی نخواهد داشت. تغییر حاصل در انرژی داخلی گاز در هر میزان گرمایش و سرمایش صفر است.
یک نکته مهم این است که یک مقدار انرژی حرارتی می تواند نه یک، بلکه چند حالت ترمودینامیکی مطابقت داشته باشد.
ماهیت تغییرات در انرژی حرارتی
برای تغییر انرژی باید کار کرد. کار را می توان توسط خود گاز یا نیروی خارجی انجام داد.
در حالت اول، صرف انرژی برای انجام کار به دلیل انرژی داخلی گاز است. مثلاً ما در یک مخزن با پیستون گاز فشرده داشتیم. اگر پیستون را رها کنید، گاز در حال انبساط شروع به بلند کردن آن می کند و کار را انجام می دهد (برای مفید بودن، اجازه دهید پیستون نوعی وزن را بلند کند). انرژی داخلی گاز با مقداری که برای کار در برابر گرانش و نیروهای اصطکاک صرف می شود کاهش می یابد: U 2 = U 1 - A. در این حالت، کار گاز مثبت است، زیرا جهت نیروی وارد شده به پیستون با جهت حرکت پیستون منطبق است.
بیایید شروع به پایین آوردن پیستون کنیم، کار را در برابر نیروی فشار گاز و دوباره در برابر نیروهای اصطکاک انجام دهیم. بنابراین مقدار معینی انرژی به گاز می دهیم. در اینجا کار نیروهای خارجی از قبل مثبت تلقی می شود.
علاوه بر کارهای مکانیکی، روشی نیز برای گرفتن انرژی از گاز یا دادن انرژی به آن وجود دارد، همانطور که قبلاً در مثال گرم کردن گاز با آن مواجه شدیم. انرژی منتقل شده به گاز در طی فرآیندهای تبادل حرارتی، مقدار گرما نامیده می شود. سه نوع انتقال حرارت وجود دارد: رسانایی، همرفتی و انتقال تابشی. بیایید با کمی جزئیات بیشتر به آنها نگاه کنیم.
رسانایی گرمایی
توانایی یک ماده برای تبادل گرما که توسط ذرات آن با انتقال انرژی جنبشی به یکدیگر در هنگام برخوردهای متقابل در حین حرکت حرارتی انجام می شود، رسانایی گرمایی است. اگر ناحیه خاصی از یک ماده گرم شود، یعنی مقدار معینی گرما به آن داده شود، انرژی درونی پس از مدتی از طریق برخورد اتم ها یا مولکول ها به طور متوسط به طور یکنواخت بین همه ذرات توزیع می شود.
واضح است که رسانایی حرارتی به شدت به فرکانس برخوردها بستگی دارد و این به نوبه خود به میانگین فاصله بین ذرات بستگی دارد. بنابراین، گاز، به ویژه گاز ایده آل، با رسانایی حرارتی بسیار پایین مشخص می شود و این خاصیت اغلب برای عایق حرارتی استفاده می شود.

از میان گازهای واقعی، رسانایی گرمایی در گازهایی که مولکولهایشان سبکترین و در عین حال چند اتمی است، بیشتر است. این شرایط تا حد زیادی توسط هیدروژن مولکولی و کمترین میزان توسط رادون به عنوان سنگین ترین گاز تک اتمی برآورده می شود. هرچه گاز کمیاب تر باشد، رسانای گرما بدتر است.
به طور کلی، انتقال انرژی توسط هدایت حرارتی برای یک گاز ایده آل، فرآیندی بسیار ناکارآمد است.
همرفت
برای گاز بسیار موثرتر همرفت است که در آن انرژی داخلی از طریق جریان ماده در حال گردش در میدان گرانشی توزیع می شود. گاز داغ به دلیل نیروی ارشمیدسی تشکیل می شود، زیرا چگالی کمتری دارد زیرا گاز داغ به سمت بالا حرکت می کند و دائماً با گاز سردتر جایگزین می شود - گردش جریان گاز برقرار می شود. بنابراین، برای اطمینان از موثرترین، یعنی سریعترین گرمایش از طریق همرفت، لازم است مخزن گاز را از زیر گرم کنید - درست مانند یک کتری با آب.
اگر لازم است مقدار معینی گرما را از گاز خارج کنید، بهتر است یخچال را در قسمت بالایی قرار دهید، زیرا گازی که به یخچال انرژی داده است تحت تأثیر گرانش به سمت پایین سرازیر می شود.
نمونه ای از همرفت در گاز، گرم کردن هوای داخل خانه با استفاده از سیستم های گرمایشی (در پایین ترین حد ممکن در اتاق قرار می گیرند) یا سرمایش با استفاده از تهویه مطبوع است و در شرایط طبیعی پدیده همرفت حرارتی باعث حرکت توده های هوا می شود و بر آب و هوا تأثیر می گذارد. و آب و هوا
در غیاب گرانش (با بی وزنی در سفینه فضایی)، همرفت، یعنی گردش جریان های هوا برقرار نمی شود. بنابراین روشن کردن مشعل های گاز یا کبریت ها در فضاپیما فایده ای ندارد: محصولات احتراق داغ به سمت بالا تخلیه نمی شوند و اکسیژن به منبع آتش نمی رسد و شعله خاموش می شود.

انتقال تابشی
یک ماده همچنین می تواند تحت تأثیر تابش حرارتی گرم شود، زمانی که اتم ها و مولکول ها با جذب کوانتوم های الکترومغناطیسی - فوتون ها انرژی می گیرند. در فرکانسهای فوتون پایین این فرآیند خیلی کارآمد نیست. به یاد داشته باشیم که وقتی مایکروفر را باز می کنیم، غذای گرم را در آنجا پیدا می کنیم، اما هوای گرم را نه. با افزایش فرکانس تابش، اثر گرمایش تشعشع افزایش می یابد، به عنوان مثال، در اتمسفر فوقانی زمین، گاز بسیار کمیاب به شدت توسط تابش فرابنفش خورشیدی یونیزه می شود.
گازهای مختلف تشعشعات حرارتی را به درجات مختلف جذب می کنند. بنابراین، آب، متان، دی اکسید کربن آن را به شدت جذب می کنند. پدیده اثر گلخانه ای بر اساس همین ویژگی است.
قانون اول ترمودینامیک
به طور کلی، تغییر در انرژی داخلی از طریق گرم کردن یک گاز (تبادل حرارتی) نیز به انجام کار بر روی مولکول های گاز یا از طریق یک نیروی خارجی (که به همان شکل، اما با علامت مخالف نشان داده می شود) منجر می شود. چه نوع کاری با این روش انتقال از یک حالت به حالت دیگر انجام می شود؟ قانون بقای انرژی به ما کمک می کند به این سوال پاسخ دهیم، یا به طور دقیق تر، مشخص کردن آن در رابطه با رفتار سیستم های ترمودینامیکی - قانون اول ترمودینامیک.
قانون یا اصل جهانی بقای انرژی در کلی ترین شکل خود بیان می کند که انرژی از هیچ زاده نمی شود و بدون اثری ناپدید نمی شود، بلکه فقط از شکلی به شکل دیگر منتقل می شود. در رابطه با یک سیستم ترمودینامیکی، این باید به گونه ای درک شود که کار انجام شده توسط سیستم از طریق تفاوت بین مقدار گرمای وارد شده به سیستم (گاز ایده آل) و تغییر در انرژی داخلی آن بیان شود. به عبارت دیگر، مقدار گرمای وارد شده به گاز صرف این تغییر و عملکرد سیستم می شود.
این به شکل فرمول بسیار ساده تر نوشته شده است: dA = dQ - dU، و بر این اساس، dQ = dU + dA.
ما قبلاً می دانیم که این کمیت ها به روشی که در آن گذار بین حالت ها رخ می دهد بستگی ندارد. سرعت این انتقال و در نتیجه کارایی به روش بستگی دارد.
در مورد قانون دوم ترمودینامیک، جهت تغییر را مشخص می کند: گرما را نمی توان از گاز سردتر (و در نتیجه کم انرژی تر) به گاز داغتر بدون صرف انرژی اضافی از بیرون منتقل کرد. قانون دوم همچنین نشان می دهد که بخشی از انرژی که توسط سیستم برای انجام کار صرف می شود، ناگزیر از بین می رود، از بین نمی رود (از بین نمی رود، اما به شکل غیرقابل استفاده می رود).
فرآیندهای ترمودینامیکی
انتقال بین حالت های انرژی یک گاز ایده آل می تواند ویژگی های متفاوتی از تغییرات در برخی از پارامترهای آن داشته باشد. انرژی داخلی در فرآیندهای انتقال انواع مختلف نیز رفتار متفاوتی خواهد داشت. اجازه دهید به طور خلاصه چندین نوع از این فرآیندها را در نظر بگیریم.

- یک فرآیند ایزوکوریک بدون تغییر در حجم رخ می دهد، بنابراین، گاز هیچ کاری انجام نمی دهد. انرژی داخلی گاز به عنوان تابعی از تفاوت بین دمای نهایی و اولیه تغییر می کند.
- یک فرآیند ایزوباریک در فشار ثابت رخ می دهد. گاز عمل می کند و انرژی حرارتی آن مانند حالت قبلی محاسبه می شود.
- یک فرآیند همدما با دمای ثابت مشخص می شود، به این معنی که انرژی حرارتی تغییر نمی کند. مقدار گرمای دریافتی توسط گاز به طور کامل صرف انجام کار می شود.
- یک فرآیند آدیاباتیک یا آدیاباتیک در یک گاز بدون انتقال حرارت، در یک ظرف عایق حرارتی رخ می دهد. کار فقط به دلیل مصرف انرژی حرارتی انجام می شود: dA = - dU. در طول فشرده سازی آدیاباتیک، انرژی حرارتی افزایش می یابد و در حین انبساط، بر این اساس کاهش می یابد.
ایزوفرایندهای مختلف زیربنای عملکرد موتورهای حرارتی هستند. بنابراین، یک فرآیند ایزوکوریک در یک موتور بنزینی در موقعیتهای انتهایی پیستون در سیلندر انجام میشود و حرکت دوم و سوم موتور نمونههایی از فرآیند آدیاباتیک هستند. هنگام تولید گازهای مایع، انبساط آدیاباتیک نقش مهمی ایفا می کند - به لطف آن، تراکم گاز امکان پذیر می شود. فرآیندهای ایزو در گازها که در مطالعه آنها نمی توان بدون مفهوم انرژی داخلی یک گاز ایده آل انجام داد، مشخصه بسیاری از پدیده های طبیعی است و در طیف گسترده ای از شاخه های فناوری کاربرد دارد.
انرژی درونیترمودینامیکی عملکرد وضعیت سیستم، انرژی آن، در داخل تعیین می شود. وضعیت. انرژی داخلی اساساً جمع می شود. از جنبشی انرژی حرکت ذرات ( , ) و انرژی برهمکنش. بین آنها (درون و بین مولکولی). انرژی درونی تحت تاثیر تغییرات انرژی درونی است. وضعیت سیستم تحت تأثیر عوامل خارجی زمینه های؛ انرژی درونی به ویژه شامل انرژی مرتبط با انرژی خارجی است. برقی میدان و مغناطیس به خارج. ماگ رشته. جنبشی. انرژی سیستم به عنوان یک کل و انرژی پتانسیل ناشی از فضا. مکان سیستم در انرژی داخلی گنجانده نشده است. B فقط با تغییر انرژی داخلی در تجزیه تعیین می شود. فرآیندها بنابراین، انرژی داخلی بسته به انرژی در نظر گرفته شده به عنوان صفر مرجع، تا یک مدت ثابت مشخص مشخص می شود.انرژی داخلی U به عنوان یک تابع حالت معرفی شده است که بر اساس آن تفاوت بین گرمای Q منتقل شده به سیستم و کار W انجام شده توسط سیستم فقط به حالت های اولیه و نهایی سیستم بستگی دارد و به مسیر انتقال بستگی ندارد. ، یعنی نشان دهنده تغییر در عملکرد حالت است
که در آن U 1 و U 2 به ترتیب انرژی داخلی سیستم در حالت اولیه و نهایی هستند. معادله (1) به صورت اعمال شده در ترمودینامیک بیان می شود. فرآیندها، یعنی فرآیندهایی که در آنها انتقال حرارت رخ می دهد. برای چرخه ای فرآیندی که سیستم را به حالت اولیه باز می گرداند. در فرآیندهای ایزوکوریک، به عنوان مثال. فرآیندهای با حجم ثابت، سیستم به دلیل انبساط کار نمی کند، W = 0 و گرمای منتقل شده به سیستم برابر با افزایش انرژی داخلی است: Q v =. برای آدیاباتیک زمانی که Q = 0، = - W پردازش می کند.
انرژی درونی سیستم به عنوان تابعی از S، حجم V و عدد m i جزء i ام است. این نتیجه اولین است و با رابطه بیان می شود:
![]() "
"
جایی که T abs است. t-ra، p-pressure، -chemical. پتانسیل مولفه i. علامت مساوی به فرآیندهای تعادلی اشاره دارد، علامت نابرابری به فرآیندهای غیرتعادلی اشاره دارد. برای سیستمی با مقادیر داده شده S، V، m i (در یک پوسته صلب آدیاباتیک)، انرژی داخلی در حداقل است. اتلاف انرژی داخلی در فرآیندهای برگشت پذیر در ثابت V و S برابر است با حداکثر. کار مفید (نگاه کنید به).
وابستگی انرژی داخلی یک سیستم تعادلی به دما و حجم U =f(T,V) نامیده می شود. کالری مشتق انرژی داخلی نسبت به دما در حجم ثابت برابر با ایزوکوریک است:
![]()
انرژی داخلی به حجم بستگی ندارد و تنها با حجم تعیین می شود.
مقدار انرژی داخلی یک ماده به صورت تجربی تعیین می شود و از مقدار آن در abs اندازه گیری می شود. صفر t-ry. تعیین انرژی داخلی به داده هایی در مورد CV (T)، گرما و سطح حالت نیاز دارد. تغییر در انرژی درونی در طول شیمی. p-tions (به ویژه انرژی داخلی استاندارد تشکیل یک ماده) از داده های مربوط به اثرات حرارتی p-tion ها و همچنین از داده های طیفی تعیین می شود. نظری محاسبه انرژی داخلی با استفاده از روش های آماری انجام می شود. ، که انرژی داخلی را به عنوان انرژی متوسط سیستم در شرایط عایق معین (مثلاً در T, V, m i معین) تعریف می کند. انرژی داخلی یک تک اتمی مجموع انرژی متوسط ورودی است. حرکت و انرژی متوسط حالات الکترونیکی برانگیخته؛ برای دو و چند اتمی، میانگین انرژی چرخش و ارتعاشات آنها در اطراف موقعیت نیز به این مقدار اضافه می شود. انرژی درونی 1
صفحه 1
انرژی درونی یک ماده، انرژی مولکول هایی است که آن ماده را تشکیل می دهند. در فرآیندهای ترمودینامیکی معمولی، تنها بخشهای جنبشی و پتانسیل انرژی داخلی دستخوش تغییرات میشوند. اولی به سرعت حرکت مولکول ها (ترجمهی، چرخشی، ارتعاشی) بستگی دارد، دومی با وجود نیروهای برهمکنش (جاذب یا دافعه) بین مولکول ها و فاصله بین آنها تعیین می شود.
انرژی درونی یک ماده، انرژی کل آن است که از انرژی های جنبشی و پتانسیل، اتم ها و مولکول های سازنده ماده و همچنین ذرات بنیادی تشکیل دهنده اتم ها و مولکول ها تشکیل شده است.
انرژی درونی یک ماده فقط به حالت فیزیکی آن بستگی دارد و به نحوه یا مسیری که یک ماده معین به آن حالت داده می شود بستگی ندارد. این به طور مستقیم از قانون بقای انرژی ناشی می شود. در واقع، اجازه دهید با اعداد 1 و 2 دو حالت دلخواه سیستم را نشان دهیم. بگذارید V انرژی صرف شده برای این انتقال باشد. اجازه دهید اکنون سیستم را مجبور کنیم که اولین انتقال را در جهت جلو و دومی را در جهت مخالف انجام دهد. در طول انتقال اول، انرژی [/ مصرف می شود، در طول دوم، U قطع می شود، بنابراین، اجسام خارجی اطراف سیستم انرژی U - V را دریافت می کنند و هیچ تغییری در خود سیستم رخ نمی دهد. U مثبت است یا منفی، مهم نیست. در هر صورت، استدلال ما ما را به تناقض با قانون بقای انرژی سوق داد.
انرژی درونی یک ماده، تحت شرایط معین، نه تنها به ماهیت شیمیایی آن، بلکه به وضعیت تجمع آن، و برای کریستال ها، به تغییر آنها بستگی دارد.
انرژی درونی یک ماده انرژی کل آن است که از انرژی جنبشی و پتانسیل اتم ها و مولکول های سازنده ماده و همچنین ذرات بنیادی تشکیل دهنده اتم ها و مولکول ها خلاصه می شود. این شامل: 1) انرژی حرکت انتقالی، چرخشی و ارتعاشی همه ذرات. 2) انرژی پتانسیل تعامل (جاذب و دافعه) بین آنها. 3) انرژی شیمیایی درون مولکولی؛ 4) انرژی درون اتمی؛ 5) انرژی درون هسته ای؛ 6) انرژی گرانشی؛ 7) انرژی تابشی که فضای اشغال شده توسط بدن را پر می کند و تعادل حرارتی را در داخل بدن بین قسمت های جداگانه آن تضمین می کند. انرژی داخلی انرژی پتانسیل را به دلیل موقعیت سیستم در فضا و انرژی جنبشی حرکت سیستم به طور کلی شامل نمی شود.
انرژی درونی یک ماده به انرژی تشعشعی تبدیل می شود.
انرژی درونی یک ماده مجموع انرژی جنبشی همه مولکول ها و انرژی های بالقوه برهمکنش بین مولکول ها است. هر چه انرژی درونی بیشتر باشد، گرمای بیشتری در بدن وجود دارد و دمای آن بالاتر می رود.
افزایش انرژی داخلی یک ماده در حین تبخیر بدون تغییر دما عمدتاً به این دلیل است که وقتی به بخار می رود ، میانگین فاصله بین مولکول ها افزایش می یابد. در همان زمان، انرژی پتانسیل آنها افزایش می یابد، زیرا برای جابجایی مولکول ها از یکدیگر در فواصل طولانی، باید برای غلبه بر نیروهای جذب مولکول ها به یکدیگر کار صرف شود.
انرژی درونی یک ماده به عنوان مجموع انرژی جنبشی حرکت مولکول ها، انرژی پتانسیل برهمکنش آنها و همچنین انرژی ارتعاش اتم ها در داخل مولکول ها درک می شود. هنگام تعیین وضعیت یک جسم، مقدار انرژی داخلی به شدت تعریف می شود، بنابراین به عنوان پارامترهای وضعیت بدن نیز طبقه بندی می شود.
در این حالت، انرژی درونی ماده به انرژی تشعشعی (انرژی فوتون ها یا امواج الکترومغناطیسی) تبدیل می شود که وقتی به اجسامی که قادر به جذب آن هستند برخورد می کند، دوباره به انرژی داخلی تبدیل می شود. به عنوان مثال، هنگامی که یک فضاپیما در فضای بین سیاره ای پرواز می کند، سطح آن تشعشعات خورشید را جذب می کند.
از آنجایی که انرژی درونی مواد تابعی از حجم، فشار و دما است، پس بدیهی است که اثرات حرارتی واکنشها به شرایطی بستگی دارد که در آن این واکنشها رخ میدهند. در عمل، تأثیر دما بر اثرات حرارتی فرآیندها از بیشترین اهمیت برخوردار است.
نشان دهید که انرژی درونی یک ماده با یک معادله حالت به شکل pTf (V) به حجم بستگی ندارد.
نشان دهید که انرژی داخلی یک ماده با یک معادله حالت به شکل p / (F) T به حجم بستگی ندارد.
با توجه به تغییرات انرژی درونی یک ماده هنگام گرم شدن، تقریباً تمام خواص فیزیکی ماده اخیر کم و بیش به دما بستگی دارد، اما برای اندازه گیری آن، در صورت امکان، آنهایی از آنها انتخاب می شوند که به وضوح با دما تغییر می کنند. ، تحت تأثیر عوامل دیگر نیستند و اندازه گیری آنها نسبتاً آسان است. این الزامات به طور کامل توسط خواص مواد عامل مانند انبساط حجمی، تغییر فشار در حجم بسته، تغییر در مقاومت الکتریکی، وقوع نیروی ترموالکتروموتور و شدت تابش برآورده می شود که اساس طراحی دستگاه های اندازه گیری دما را تشکیل می دهد. .
انرژی یک معیار کلی برای اشکال مختلف حرکت ماده است. با توجه به اشکال حرکت ماده، انواع انرژی نیز متمایز می شود - مکانیکی، الکتریکی، شیمیایی و غیره. هر سیستم ترمودینامیکی در هر حالتی دارای مقدار معینی انرژی است که وجود آن توسط R. Clausius (1850) اثبات شد و انرژی درونی نامیده شد.
انرژی درونی (U) انرژی همه انواع حرکت ریزذرات تشکیل دهنده سیستم و انرژی برهمکنش آنها با یکدیگر است.
انرژی درونی شامل انرژی حرکت انتقالی، چرخشی و ارتعاشی ذرات، انرژی برهمکنش های بین مولکولی و درون مولکولی، درون اتمی و درون هسته ای و غیره است.
انرژی برهمکنش درون مولکولی، یعنی. انرژی برهمکنش اتم ها در یک مولکول که اغلب نامیده می شود انرژی شیمیایی . تغییر در این انرژی در طول تبدیلات شیمیایی رخ می دهد.
برای آنالیز ترمودینامیکی، نیازی به دانستن اینکه انرژی درونی از کدام اشکال حرکت ماده تشکیل شده است، نیست.
مقدار انرژی داخلی فقط به وضعیت سیستم بستگی دارد. در نتیجه، انرژی درونی را می توان به عنوان یکی از ویژگی های این حالت در کنار مقادیری مانند فشار، دما در نظر گرفت.
هر حالت سیستم مربوط به یک مقدار کاملاً تعریف شده از هر یک از ویژگی های آن است.
اگر یک سیستم همگن در حالت اولیه دارای حجم V 1، فشار P 1، دمای T 1، انرژی داخلی U 1، هدایت الکتریکی æ 1 و غیره باشد و در حالت نهایی این خواص به ترتیب برابر با V 2، P 2 باشد. ، T 2، U 2، æ 2 و غیره، سپس تغییر در هر ویژگی در هنگام انتقال سیستم از حالت اولیه به حالت نهایی یکسان خواهد بود، صرف نظر از اینکه سیستم از یک حالت به حالت دیگر عبور می کند. : اول، دوم یا سوم (شکل .1.4).
برنج. 1.4 استقلال ویژگی های سیستم از مسیر انتقال آن
از حالت عادی به حالت دیگر
آن ها (U 2 - U 1) I = (U 2 - U 1) II = (U 2 - U 1) III (1.4)
اعداد I، II، III و غیره کجا هستند. مسیرهای فرآیند را نشان می دهد. در نتیجه، اگر سیستم از حالت اولیه (1) به حالت نهایی (2) در طول یک مسیر و از حالت نهایی در ابتدا - در طول مسیر دیگری حرکت کند، یعنی. اگر یک فرآیند (چرخه) دایره ای کامل شود، تغییر در هر ویژگی سیستم برابر با صفر خواهد بود.
بنابراین، تغییر در تابع حالت سیستم به مسیر فرآیند بستگی ندارد، بلکه تنها به حالت های اولیه و نهایی سیستم بستگی دارد. یک تغییر بی نهایت کوچک در خواص یک سیستم معمولاً با علامت دیفرانسیل d نشان داده می شود. به عنوان مثال، dU یک تغییر بی نهایت کوچک در انرژی داخلی و غیره است.
اشکال تبادل انرژی
مطابق با اشکال مختلف حرکت ماده و انواع مختلف انرژی، اشکال مختلفی از تبادل انرژی (انتقال انرژی) - اشکال تعامل وجود دارد. ترمودینامیک دو شکل تبادل انرژی بین یک سیستم و محیط آن را در نظر می گیرد. این کار و گرمی است.
کار.واضح ترین شکل تبادل انرژی، کار مکانیکی است که مطابق با شکل مکانیکی حرکت ماده است. هنگامی که بدن تحت تأثیر نیروی مکانیکی حرکت می کند تولید می شود. مطابق با سایر اشکال حرکت ماده، انواع دیگر کار نیز متمایز می شود: الکتریکی، شیمیایی و غیره. کار نوعی انتقال حرکت منظم و سازمان یافته است، زیرا هنگام انجام کار، ذرات بدن به صورت سازمان یافته در یک جهت حرکت می کنند. به عنوان مثال، کار انجام شده در حین انبساط گاز. مولکول های گاز واقع در سیلندر زیر پیستون در حرکت بی نظم و بی نظم هستند. هنگامی که گاز شروع به حرکت پیستون می کند، یعنی برای انجام کار مکانیکی، حرکت سازمان یافته بر حرکت تصادفی مولکول های گاز سوار می شود: همه مولکول ها مقداری جابجایی در جهت حرکت پیستون دریافت می کنند. کار الکتریکی همچنین با حرکت سازمان یافته ذرات باردار ماده در جهت خاصی همراه است.
از آنجایی که کار اندازه گیری انرژی منتقل شده است، کمیت آن با همان واحدهای انرژی اندازه گیری می شود.
حرارت. شکل تبادل انرژی مربوط به حرکت آشفته ریز ذرات تشکیل دهنده سیستم نامیده می شود تبادل حرارت، و مقدار انرژی منتقل شده در هنگام تبادل حرارت نامیده می شود گرما.
انتقال حرارت با تغییر در موقعیت اجسامی که یک سیستم ترمودینامیکی را تشکیل میدهند ارتباطی ندارد و شامل انتقال مستقیم انرژی از مولکولهای یک جسم به مولکولهای جسم دیگر در تماس آنهاست.
پ  اجازه دهید یک مخزن (سیستم) عایق را تصور کنیم که توسط یک پارتیشن رسانای گرما AB به دو قسمت تقسیم شده است (شکل 1.5). فرض کنید در هر دو قسمت ظرف گاز وجود دارد.
اجازه دهید یک مخزن (سیستم) عایق را تصور کنیم که توسط یک پارتیشن رسانای گرما AB به دو قسمت تقسیم شده است (شکل 1.5). فرض کنید در هر دو قسمت ظرف گاز وجود دارد.
برنج. 1.5. به مفهوم گرما
در نیمه چپ ظرف دمای گاز T 1 و در نیمه سمت راست T 2 است. اگر T 1 > T 2، آنگاه انرژی جنبشی متوسط (  ) مولکول های گاز در سمت چپ ظرف بزرگتر از میانگین انرژی جنبشی خواهند بود (
) مولکول های گاز در سمت چپ ظرف بزرگتر از میانگین انرژی جنبشی خواهند بود (  ) در نیمه سمت راست رگ.
) در نیمه سمت راست رگ.
در نتیجه برخورد مداوم مولکول ها با پارتیشن در نیمه چپ رگ، بخشی از انرژی آنها به مولکول های پارتیشن منتقل می شود. مولکول های گاز واقع در نیمه سمت راست ظرف، در برخورد با پارتیشن، بخشی از انرژی را از مولکول های آن به دست می آورند.
در نتیجه این برخوردها، انرژی جنبشی مولکول ها در نیمه چپ رگ کاهش می یابد و در نیمه سمت راست افزایش می یابد. دماهای T 1 و T 2 برابر خواهند شد.
از آنجایی که گرما شکلی از انرژی است، کمیت آن با واحدهای انرژی اندازه گیری می شود. بنابراین تبادل گرما و کار اشکال تبادل انرژی هستند و مقدار گرما و مقدار کار معیارهای انرژی منتقل شده است. تفاوت آنها در این است که گرما شکلی از انتقال حرکت میکروفیزیکی و بی نظم ذرات (و بر این اساس، انرژی این حرکت) است و کار شکلی از انتقال انرژی حرکت منظم و سازمان یافته ماده است.
گاهی می گویند: گرما (یا کار) از سیستم تامین یا حذف می شود، اما باید فهمید که تامین یا حذف گرما و کار نیست، بلکه انرژی است، بنابراین نباید از عباراتی مانند ذخیره گرما استفاده کرد. یا «حاوی گرما».
به عنوان اشکال تبادل انرژی (اشکال برهمکنش) یک سیستم با محیط، گرما و کار نمی توانند با هیچ حالت خاصی از سیستم مرتبط باشند، نمی توانند خواص آن و بنابراین عملکردهای حالت آن باشند. این بدان معنی است که اگر سیستم از حالت اولیه (1) به حالت نهایی (2) به روش های مختلف عبور کند، گرما و کار مقادیر متفاوتی برای مسیرهای انتقال مختلف خواهند داشت (شکل 1.6).

مقادیر متناهی گرما و کار به ترتیب با Q و A و مقادیر بینهایت کوچک با δQ و δA نشان داده می شوند. کمیتهای δQ و δA، بر خلاف dU، یک دیفرانسیل کامل نیستند، زیرا Q و A توابع حالت نیستند.
هنگامی که مسیر فرآیند از پیش تعیین شده باشد، کار و گرما ویژگی های عملکردهای حالت سیستم را به دست می آورند، یعنی. مقادیر عددی آنها فقط با حالت اولیه و نهایی سیستم تعیین می شود.
سرفصل های کد آزمون دولتی واحد: انرژی داخلی، انتقال حرارت، انواع انتقال حرارت.
ذرات هر جسم - اتم ها یا مولکول ها - حرکت مداوم بی نظم را انجام می دهند (به اصطلاح حرکت حرارتی). بنابراین، هر ذره مقداری انرژی جنبشی دارد.
علاوه بر این، ذرات ماده از طریق نیروهای جاذبه و دافعه الکتریکی و همچنین از طریق نیروهای هسته ای با یکدیگر تعامل دارند. بنابراین، کل سیستم ذرات یک جسم معین نیز دارای انرژی بالقوه است.
انرژی جنبشی حرکت حرارتی ذرات و انرژی پتانسیل تعامل آنها با هم نوع جدیدی از انرژی را تشکیل می دهند که به انرژی مکانیکی بدن کاهش نمی یابد (یعنی انرژی جنبشی حرکت بدن به عنوان یک کل و انرژی پتانسیل تعامل آن با سایر اجسام). به این نوع انرژی انرژی داخلی می گویند.
انرژی درونی یک جسم مجموع انرژی جنبشی حرکت حرارتی ذرات آن به اضافه انرژی پتانسیل برهمکنش آنها با یکدیگر است..
انرژی داخلی یک سیستم ترمودینامیکی مجموع انرژی های داخلی اجسام موجود در سیستم است..
بنابراین انرژی درونی بدن با عبارات زیر تشکیل می شود.
1. انرژی جنبشی حرکت آشفته پیوسته ذرات بدن.
2. انرژی بالقوه مولکول ها (اتم ها)، ناشی از نیروهای برهمکنش بین مولکولی.
3. انرژی الکترون ها در اتم ها.
4. انرژی درون هسته ای.
در مورد ساده ترین مدل ماده - یک گاز ایده آل - می توان یک فرمول صریح برای انرژی داخلی به دست آورد.
انرژی داخلی یک گاز ایده آل تک اتمی
انرژی پتانسیل برهمکنش بین ذرات یک گاز ایده آل صفر است (به یاد بیاورید که در مدل گاز ایده آل از برهمکنش ذرات در فاصله چشم پوشی می کنیم). بنابراین، انرژی داخلی یک گاز ایده آل تک اتمی به کل انرژی جنبشی انتقالی (برای گاز چند اتمی باید چرخش مولکول ها و ارتعاشات اتم ها در داخل مولکول ها را نیز در نظر گرفت) حرکت اتم های آن کاهش می یابد. این انرژی را می توان با ضرب تعداد اتم های گاز در میانگین انرژی جنبشی یک اتم پیدا کرد:
می بینیم که انرژی داخلی یک گاز ایده آل (که جرم و ترکیب شیمیایی آن بدون تغییر است) فقط تابع دمای آن است. در گاز، مایع یا جامد واقعی، انرژی داخلی نیز به حجم بستگی دارد - از این گذشته، هنگامی که حجم تغییر می کند، آرایش نسبی ذرات و در نتیجه، انرژی پتانسیل تعامل آنها تغییر می کند.
تابع وضعیت
مهمترین خاصیت انرژی درونی این است که هست تابع حالتسیستم ترمودینامیکی یعنی انرژی داخلی به طور منحصر به فردی توسط مجموعه ای از پارامترهای ماکروسکوپی مشخص کننده سیستم تعیین می شود و به "پیش تاریخ" سیستم بستگی ندارد. در مورد اینکه سیستم قبلاً در چه وضعیتی بود و به طور خاص چگونه در این وضعیت قرار گرفت.
بنابراین، هنگامی که یک سیستم از یک حالت به حالت دیگر منتقل می شود، تغییر انرژی درونی آن تنها توسط حالت های اولیه و نهایی سیستم تعیین می شود. وابسته نیستاز مسیر انتقال از حالت اولیه به حالت نهایی. اگر سیستم به حالت اولیه خود بازگردد، تغییر در انرژی داخلی آن صفر است.
تجربه نشان می دهد که تنها دو راه برای تغییر انرژی درونی بدن وجود دارد:
انجام کارهای مکانیکی؛
انتقال حرارت.
به عبارت ساده، شما می توانید یک کتری را فقط به دو روش کاملاً متفاوت گرم کنید: مالش آن با چیزی یا آتش زدن آن :-) بیایید این روش ها را با جزئیات بیشتری در نظر بگیریم.
تغییر در انرژی درونی: کار انجام شده
اگر کار انجام شود در بالابدن، سپس انرژی درونی بدن افزایش می یابد.
به عنوان مثال، پس از ضربه زدن با چکش، میخ گرم می شود و کمی تغییر شکل می دهد. اما دما معیاری از میانگین انرژی جنبشی ذرات در یک جسم است. گرم کردن میخ نشان دهنده افزایش انرژی جنبشی ذرات آن است: در واقع ذرات با ضربه چکش و اصطکاک میخ روی تخته شتاب می گیرند.
تغییر شکل چیزی نیست جز جابجایی ذرات نسبت به یکدیگر. پس از ضربه، یک میخ تغییر شکل فشاری را تجربه می کند، ذرات آن به هم نزدیک می شوند، نیروهای دافعه بین آنها افزایش می یابد و این منجر به افزایش انرژی بالقوه ذرات ناخن می شود.
بنابراین انرژی داخلی ناخن افزایش یافته است. این نتیجه کار روی آن بود - کار توسط چکش و نیروی اصطکاک روی تخته انجام شد.
اگر کار انجام شود خودمانبدن، سپس انرژی درونی بدن کاهش می یابد.
به عنوان مثال، اجازه دهید هوای فشرده در یک مخزن عایق حرارتی زیر یک پیستون منبسط شود و بار خاصی را بلند کند، در نتیجه کار انجام می شود (فرایند در یک مخزن عایق حرارتی نامیده می شود. آدیاباتیک. ما فرآیند آدیاباتیک را با در نظر گرفتن قانون اول ترمودینامیک مطالعه خواهیم کرد). در طی این فرآیند، هوا خنک می شود - مولکول های آن که پس از پیستون متحرک ضربه می زنند، بخشی از انرژی جنبشی خود را به آن می دهند. (به همین ترتیب یک بازیکن فوتبال در حالی که با پا توپی را که سریع پرواز می کند متوقف می کند، با آن حرکت می کند. از جانبتوپ و سرعت آن را کاهش می دهد.) بنابراین انرژی داخلی هوا کاهش می یابد.
بنابراین، هوا با هزینه انرژی داخلی خود کار می کند: از آنجایی که کشتی از نظر حرارتی عایق است، هیچ جریانی از هیچ منبع خارجی به هوا وجود ندارد و هوا فقط می تواند از ذخایر خود انرژی برای انجام کار بگیرد. .
تغییر در انرژی داخلی: انتقال حرارت
انتقال حرارت فرآیند انتقال انرژی داخلی از یک جسم گرمتر به یک جسم سردتر است که با عملکرد مکانیکی مرتبط نیست.. انتقال حرارت می تواند از طریق تماس مستقیم اجسام یا از طریق یک محیط میانی (و حتی از طریق خلاء) رخ دهد. انتقال حرارت نیز نامیده می شود تبادل حرارت.
سه نوع انتقال حرارت وجود دارد: رسانایی، همرفت و تابش حرارتی.
اکنون با جزئیات بیشتری به آنها نگاه خواهیم کرد.
رسانایی گرمایی
اگر یک سر میله آهنی را داخل آتش بگذارید، همانطور که می دانیم آن را برای مدت طولانی در دست نخواهید داشت. هنگامی که در یک منطقه با دمای بالا قرار می گیرند، اتم های آهن با شدت بیشتری شروع به ارتعاش می کنند (یعنی انرژی جنبشی بیشتری به دست می آورند) و تأثیرات قوی تری بر همسایگان خود ایجاد می کنند.
انرژی جنبشی اتم های همسایه نیز افزایش می یابد و اکنون این اتم ها انرژی جنبشی بیشتری به همسایگان خود می دهند. بنابراین، از بخش به بخش، گرما به تدریج در امتداد میله پخش می شود - از انتهای قرار داده شده در آتش تا دست ما. این هدایت حرارتی است (شکل 1) (تصویر از Educationalelectronicsusa.com).

برنج. 1. هدایت حرارتی
رسانایی حرارتی انتقال انرژی داخلی از نواحی گرمتر بدن به مناطق کمتر گرمتر به دلیل حرکت حرارتی و تعامل ذرات بدن است..
هدایت حرارتی مواد مختلف متفاوت است. فلزات رسانایی حرارتی بالایی دارند: بهترین هادی های حرارتی نقره، مس و طلا هستند. هدایت حرارتی مایعات بسیار کمتر است. گازها به قدری ضعیف گرما را هدایت می کنند که به عنوان عایق حرارت در نظر گرفته می شوند: مولکول های گاز به دلیل فواصل زیاد بین آنها، برهمکنش ضعیفی با یکدیگر دارند. به همین دلیل است که، برای مثال، پنجره ها دارای قاب دوتایی هستند: یک لایه هوا از خروج گرما جلوگیری می کند.
بنابراین، اجسام متخلخل مانند آجر، پشم پنبه یا خز رسانای ضعیف گرما هستند. آنها حاوی هوا در منافذ خود هستند. بی جهت نیست که خانه های آجری گرم ترین خانه ها در نظر گرفته می شوند و در هوای سرد مردم کت و کت خز با لایه ای از روکش یا روکش مصنوعی می پوشند.
اما اگر هوا اینقدر ضعیف گرما را هدایت می کند، پس چرا اتاق از رادیاتور گرم می شود؟
این به دلیل نوع دیگری از انتقال حرارت - همرفت - اتفاق می افتد.
همرفت
همرفت انتقال انرژی داخلی در مایعات یا گازها در نتیجه گردش جریان ها و اختلاط مواد است..
هوای نزدیک باتری گرم شده و منبسط می شود. نیروی گرانش وارد بر این هوا ثابت می ماند، اما نیروی شناوری از هوای اطراف افزایش می یابد، به طوری که هوای گرم شده شروع به شناور شدن به سمت سقف می کند. به جای آن هوای سرد می آید (همان فرآیند، اما در مقیاسی بسیار بزرگتر، دائماً در طبیعت رخ می دهد: باد اینگونه به وجود می آید) که با آن همان چیز تکرار می شود.
در نتیجه، گردش هوا برقرار می شود، که به عنوان نمونه ای از همرفت عمل می کند - انتشار گرما در اتاق توسط جریان های هوا انجام می شود.
یک فرآیند کاملا مشابه را می توان در مایعات مشاهده کرد. هنگامی که یک کتری یا تابه آب را روی اجاق گاز قرار می دهید، آب در درجه اول به دلیل همرفت گرم می شود (سهم هدایت حرارتی آب بسیار ناچیز است).
جریانهای همرفتی در هوا و مایع در شکل نشان داده شده است. 2 (تصاویر از physics.arizona.edu).
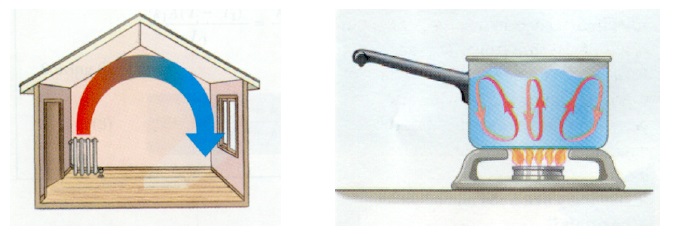
برنج. 2. همرفت
در جامدات، جابجایی وجود ندارد: نیروهای برهمکنش بین ذرات زیاد است، ذرات در نزدیکی نقاط مکانی ثابت (گرههای شبکه کریستالی) نوسان میکنند و هیچ جریانی از ماده در چنین شرایطی تشکیل نمیشود.
برای گردش جریان های همرفت هنگام گرم کردن یک اتاق، لازم است که هوای گرم شده باشد جا برای ظهور وجود داشت. اگر رادیاتور زیر سقف نصب شود، هیچ گردشی رخ نمی دهد - هوای گرم زیر سقف باقی می ماند. به همین دلیل وسایل گرمایشی قرار داده می شود در پاییناتاق ها به همین دلیل کتری روی آن گذاشته می شود برآتش، در نتیجه لایه های گرم آب که بالا می روند، جای خود را به لایه های سردتر می دهند.
برعکس، تهویه مطبوع باید تا حد امکان بالا قرار گیرد: سپس هوای خنک شده شروع به پایین آمدن می کند و هوای گرم تری جای آن را می گیرد. گردش خون در مقایسه با حرکت جریان در هنگام گرم کردن اتاق در جهت مخالف حرکت می کند.
تابش حرارتی
زمین چگونه از خورشید انرژی دریافت می کند؟ هدایت حرارتی و همرفت مستثنی شده اند: ما با 150 میلیون کیلومتر فضای بدون هوا از هم جدا شده ایم.
نوع سوم انتقال حرارت در اینجا کار می کند - تابش حرارتی. تابش می تواند هم در ماده و هم در خلاء منتشر شود. چگونه بوجود می آید؟
به نظر می رسد که میدان های الکتریکی و مغناطیسی ارتباط نزدیکی با یکدیگر دارند و دارای یک ویژگی قابل توجه هستند. اگر میدان الکتریکی با زمان تغییر کند، میدان مغناطیسی ایجاد میکند، که به طور کلی، با زمان نیز تغییر میکند (این مورد با جزئیات بیشتر در برگه القای الکترومغناطیسی مورد بحث قرار خواهد گرفت). به نوبه خود، یک میدان مغناطیسی متناوب یک میدان الکتریکی متناوب ایجاد می کند که دوباره یک میدان مغناطیسی متناوب ایجاد می کند که دوباره یک میدان الکتریکی متناوب ایجاد می کند.
در نتیجه توسعه این فرآیند، موج الکترومغناطیسی- میدان های الکتریکی و مغناطیسی "درگیر" با یکدیگر. امواج الکترومغناطیسی مانند صدا دارای سرعت انتشار و فرکانس هستند - در این مورد، این فرکانس است که با آن بزرگی و جهت میدان ها در موج نوسان می کند. نور مرئی یک مورد خاص از امواج الکترومغناطیسی است.
سرعت انتشار امواج الکترومغناطیسی در خلاء بسیار زیاد است: کیلومتر بر ثانیه. بنابراین، نور در کمتر از یک ثانیه از زمین به ماه می رسد.
محدوده فرکانس امواج الکترومغناطیسی بسیار گسترده است. در بروشور مربوطه در مورد مقیاس امواج الکترومغناطیسی بیشتر صحبت خواهیم کرد. در اینجا فقط توجه می کنیم که نور مرئی محدوده کوچکی از این مقیاس است. در زیر آن فرکانس های تابش مادون قرمز، در بالای آن فرکانس های تابش فرابنفش قرار دارد.
اکنون به یاد بیاورید که اتم ها، در حالی که عموماً از نظر الکتریکی خنثی هستند، حاوی پروتون هایی با بار مثبت و الکترون هایی با بار منفی هستند. این ذرات باردار، همراه با اتم ها، حرکات آشفته ای انجام می دهند، میدان های الکتریکی متناوب ایجاد می کنند و در نتیجه امواج الکترومغناطیسی ساطع می کنند. این امواج نامیده می شوند تابش حرارتی- به عنوان یادآوری که منبع آنها حرکت حرارتی ذرات ماده است.
هر جسمی منبع تابش حرارتی است. در این حالت تابش بخشی از انرژی درونی آن را می برد. پس از برخورد با اتم های جسم دیگری، تابش با میدان الکتریکی نوسانی خود آنها را شتاب می دهد و انرژی درونی این جسم افزایش می یابد. اینگونه است که ما در برابر اشعه های خورشید غرق می شویم.
در دمای معمولی، فرکانس تابش حرارتی در محدوده مادون قرمز قرار دارد، بنابراین چشم آن را درک نمی کند (ما نمی بینیم که چگونه "درخشش" می کنیم). هنگامی که یک جسم گرم می شود، اتم های آن شروع به انتشار امواجی با فرکانس های بالاتر می کنند. میخ آهنی را می توان به رنگ قرمز گرم کرد - به دمایی رساند که تابش حرارتی آن به قسمت پایین (قرمز) محدوده مرئی برسد. و خورشید برای ما زرد مایل به سفید به نظر می رسد: دمای سطح خورشید به قدری بالا است که طیف تابش آن شامل تمام فرکانس های نور مرئی و حتی فرابنفش است که به لطف آن برنزه می شویم.
بیایید نگاهی دیگر به سه نوع انتقال حرارت بیندازیم (شکل 3) (تصاویر از beodom.com).

برنج. 3. سه نوع انتقال حرارت: هدایت، همرفت و تابش

